胰腺癌科研进展|Science Advances讲述器官芯片革新胰腺癌研究
目前,胰腺癌患者确诊后五年生存率还不到9%,因此胰腺癌也被称为“癌中之强者”。胰腺癌难治一个原因是在胰腺癌早期,癌细胞便能够从其原发部位逃逸并转移到身体其它部位。然而,令人疑惑的,胰腺肿瘤组织缺乏血管,而癌细胞往往需要通过侵袭血管来进行扩散。
近日,来自哈佛大学、波士顿大学和宾夕法尼亚大学的一项新研究终于揭开了这个谜团。利用胰腺癌和血管系统的体外和体内模型,研究人员发现胰腺癌细胞可以侵入附近的血管,破坏内皮细胞,并用肿瘤排列成的管道替换了血管内皮细胞。这一过程的发生是由胰腺癌细胞表面的ALK7和活跃素(Activin)之间的相互作用驱动的,阻断这一信号传导途径将为胰腺癌的治疗提供一种新的方法。
该项研究表明治疗胰腺癌之前“挽救”血管系统的重要性,因为癌细胞会破坏向转移性肿瘤组织输送药物的现有途径。如果能够开发一种针对ALK7活化素途径的抑制剂,防止癌症对血管内皮细胞的清除,就可以避免肿瘤组织中血管系统被破坏,进而更好的向患者肿瘤递送药物来抑制肿瘤生长,而已有的治疗方案很难实现这一点。

研究胰腺癌和血管之间的相互作用会遇到很多障碍,因为这需要对癌症患者进行多个、侵入性的组织活检,如果是在小鼠模型中进行研究,成像技术将是个很大的挑战。因此,研究人员采用了一种不同的方法——器官芯片。器官芯片是一种透明的、功能灵活的塑料芯片,大小相当于一个U盘,芯片内部有包被了胶原蛋白的微流体通道,可以让 附着,并可通过通道中不断流动的培养基为细胞生长提供营养。
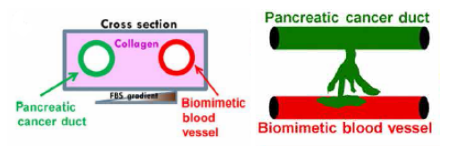
胰腺癌器官芯片示意图。左图为芯片横切面,右图为纵切面。红色表示血管内皮细胞通道,绿色表示胰腺癌细胞管道。胰腺癌细胞可以通过两个管道之间的胶原蛋白侵入内皮细胞管道
为了在芯片中构建研究胰腺癌和血管相互作用模型,研究人员在一个通道植入小鼠胰腺癌细胞,在另一个通道植入人体内皮细胞。大约四天后,胰腺癌细胞开始通过胶原基质向生长有血管的通道入侵,并较终侵入血管。在侵袭过程中,与癌细胞直接接触的内皮细胞发生凋亡(细胞死亡),导致血管通道完全由癌细胞组成。他们在器官芯片和人类胰腺癌细胞的小鼠模型中也观察到了同样的结果,这表明这种现象在人类胰腺癌中也可能存在。
研究人员假设胰腺癌细胞清除内皮细胞的机制与TGF-β信号通路有关。TGF-β信号通路是一系列分子级联反应,并与多种癌症有关。他们将一种TGF-β抑制剂加入癌症模型的器官芯片中,发现内皮细胞的清除明显减少。相同的TGF-β抑制剂注入胰腺癌小鼠模型后,肿瘤组织具有更高的血管密度,这说明TGF-β抑制剂可以在体外和体内抑制胰腺癌细胞对内皮细胞的清除。
器官芯片模型中胰腺癌细胞侵入血管内皮细胞。绿色为胰腺癌细胞,红色为内皮细胞,黄色虚线表示器官芯片的内皮细胞管道。i表示加入TGF-β抑制剂的内皮细胞管道。ii表示加入DMSO对照的内皮细胞通道
为进一步深入研究导致癌细胞清除内皮细胞的TGF-β受体,研究人员创造了一种共培养装置,在其中胰腺细胞被内皮细胞包围,如此便能直接研究两种类型的细胞相互作用。较终,他们鉴定出了三个候选受体——ALK4、ALK5和ALK7。随后,他们分别删除了内皮细胞和胰腺癌细胞的三个受体的编码基因。结果表明,只有从癌细胞中删除ALK7才能显著减少内皮细胞的清除,并减缓癌细胞的生长。
ALK7受体有两个已知的配体,即Activin和Nodal,当研究人员将癌细胞暴露于这两种配体化合物时,只有Activin减少了内皮细胞的清除,这表明ALK7和Activin之间的相互作用导致了胰腺癌的生长和转移。随后,研究人员敲除了癌细胞的ALK7基因,并构建了小鼠模型,结果进一步证实了这一点,小鼠体内肿瘤生长更慢,血管密度更高,凋亡的内皮细胞更少。
“我们的研究不仅揭示了胰腺癌转移的重要机理,为新疗法的发展提供了支撑。而且,血管与其它类型癌症之间复杂的相互作用是胰腺癌生物学的关键所在,我们开发的芯片平台为这方面的研究打开了一扇新的门。”共同第一作者Esak Lee博士说道。
目前,该团队正在积极开发他们的器官芯片平台,以进一步了解癌细胞与其它细胞相互作用,包括癌细胞和免疫细胞之间的相互作用,以及癌细胞和支持血管的血管周细胞之间的相互作用。
该研究通讯作者Chris Chen表示,“这项研究证明了3-D和2-D器官模型在疾病研究中的优势,它可以在体外复制疾病状态并可以精细准确的研究疾病的机理,这是传统的体外和体内研究方法无法比拟的。我们现在进行的研究所接触的只是浅层的,通过这个平台,我们可以发现新的机制,这将为我们提供新的更好的治疗方案。”
传统治疗方案往往靶向血管生成、免疫细胞或癌细胞本身,而该研究打破了传统的思路,通过构建的器官芯片模型发现了新的靶点,对该靶点的阻断可以防止胰腺癌细胞在血管中的定植以及进一步的转移,有望将胰腺癌困在原发部位。同时,也保护了血管系统,使其它药物更好的进入肿瘤组织中。
荐 相关文章
 手机端查看更多优质内容
手机端查看更多优质内容
在线预约
绿色快速预约通道
阅读排行